Analyses quantitative et qualitative de l'ADN
Objectifs et méthodes
La quantification de l'ADN permet de déterminer la concentration, la qualité et parfois l'intégrité de l'ADN. Plusieurs méthodes existent, dont les trois principales se font :
- par quantification sur gel d'agarose,
- par spectrophotométrie UV,
- par fluorimétrie.
Chacune de ces méthodes présente des avantages et des limites et leur choix dépend des besoins spécifiques de l'expérience en cours.
Quantification de l'ADN sur gel d'agarose
La quantification sur gel d'agarose est une méthode simple de détection visuelle qui est souvent utilisée en laboratoire pour estimer la concentration d'ADN tout en vérifiant son intégrité.
Pour ce faire, un échantillon d'ADN est analysé après migration sur un gel d'agarose. La quantification est réalisée par comparaison de l'intensité de fluorescence de l'ADN « coloré » avec un intercalant avec celle d'un marqueur de taille et de concentration connue.
La visualisation directe de l'ADN permet de contrôler également son intégrité (absence de smear) et de détecter d'éventuels contaminants. Il n'y a pas besoin d'équipement spécifiques hors le transilluminateur.
Ainsi, après migration de l'ADN, le gel est incubé avec un marqueur fluorescent puis exposé aux UV. Le marqueur émet alors une fluorescence dans le visible qui permet de détecter l'ADN.
La quantification de l'ADN est réalisée avec la comparaison de l'intensité de fluorescence des bandes d'ADN étudiées avec celles d'un marqueur de taille du commerce qui contient des fragments d'ADN de taille et de concentration connue.
Un marqueur de taille (ladder), mélange de fragments d'ADN de taille connues, permet d'estimer la taille des fragments par comparaison des distances de migration. Cette estimation n'est valable que pour des fragments linéaires.

Exemples de deux marqueur de taille:

- Piste A: gene Ruler 1kb de Thermo ScientificTM
- Piste B : Echelle de taille et de masse moléculaire d’ADN de Jeulin
Avantages et limites
La quantification sur gel d'agarose est peu précise pour les faibles concentrations (<5µg/mL) et il est important de comparer les fragments d'ADN avec des bandes du ladder de taille voisine pour conserver le même rapport entre molécules fluorescentes et taille de l'ADN.
Quantification de l'ADN par spectrophotométrie UV
L'ADN absorbe la lumière UV avec un pic d'absorption à 260nm (pic d’absorption des bases azotées). La concentration est calculée à partir de la mesure de l'absorbance à 260n, selon la loi de Beer-Lambert qui stipule que l'absorbance d'une solution est proportionnelle à la concentration de la substance absorbante et à la longueur du trajet optique traversé par la lumière.
Ainsi, à une longueur d'onde donnée la loi s'écrit :
A = ε x l x C
avec :
- A : est l’absorbance ou la densité optique de la solution (sans unité) .
- ε : est le coefficient d’extinction molaire de la substance absorbante (en L.mole−1.cm−1). Dans le cas des acides nucléiques des approximations sont effectuées (voir plus loin).
- l : est la longueur du trajet optique (en cm).
- C : est la concentration de la substance absorbante (en mole.L-1).
En pratique, il est admis de calculer les concentrations des acides nucléiques avec des coefficients d'extinction molaire (ε) approximatifs, avec les valeurs suivantes :
- pour ADN double brin, ε = 50ng.cm/µL
- pour ADN simple brin, ε = 33ng.cm/µL
- pour ARN, ε = 40ng.cm/µL
Ainsi, la concentration de l'ADN double brin est calculée selon la formule:
Concentration(µg/mL)=A260 x facteur de dilution x 50
Pour un échantillon non dilué il suffit donc de multiplier la valeur d'absorbance par 50 pour obtenir la concentration d'ADN en µg/mL.
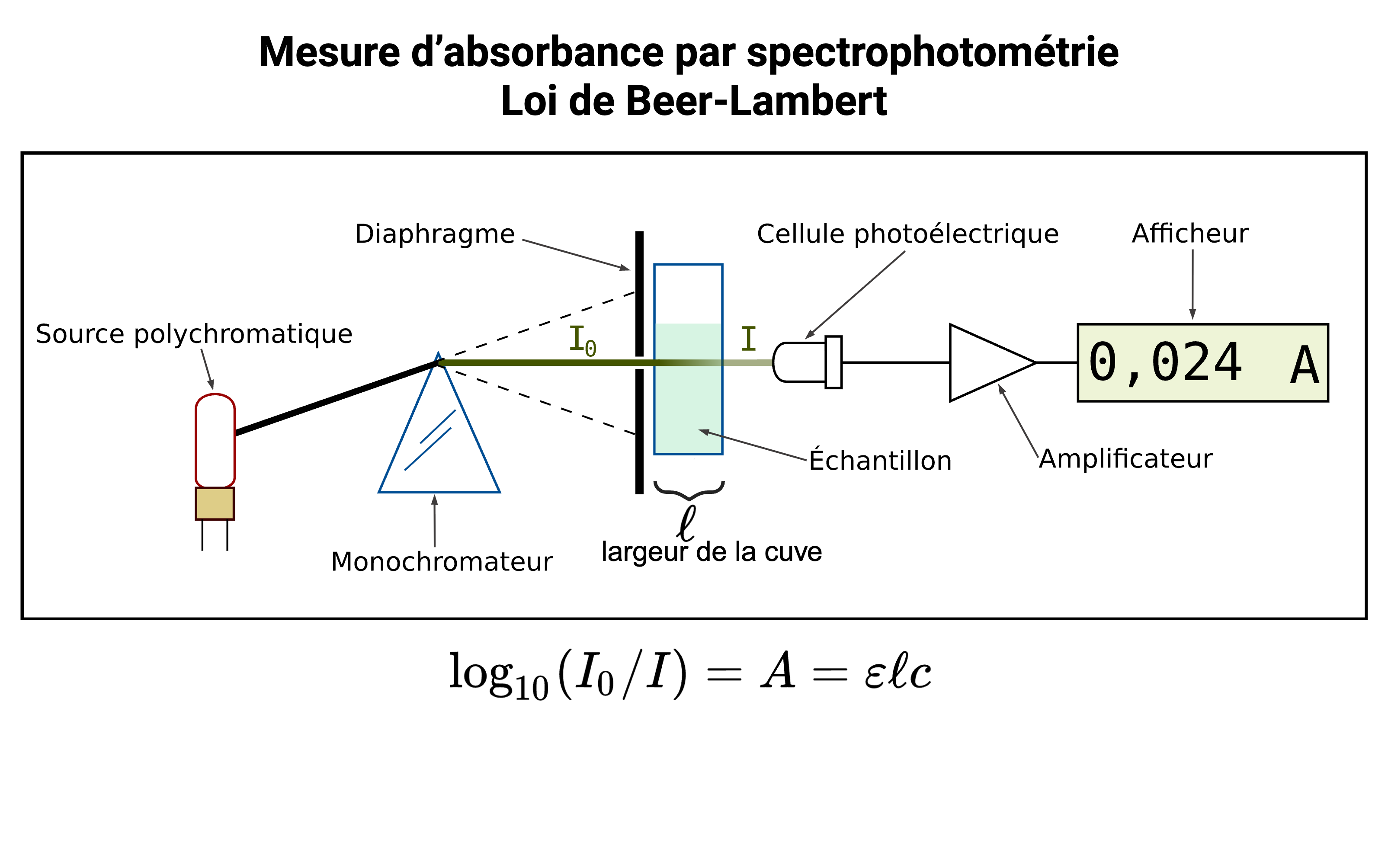
Loi de Beer-Lambert
La loi de Beer-Lambert relie l'intensité de la lumière entrante (Io) à l'intensité de la lumière sortante (I) et à la concentration de la substance qui absorbe la lumière (C). La quantité de lumière absorbée dépend de la concentration de la substance absorbante, mais aussi de la longueur d'onde (lambda) de la lumière entrante ou incidente. La distance parcourue par la lumière à travers la substance absorbante (l) qui est la largeur de la cuve de mesure.
Estimation de la pureté de l'ADN.
La mesure de l'absorbance de l'ADN permet également d'évaluer la pureté de l'échantillon d'ADN grâce au rapport A260/A280. En effet, la mesure à 260nm peut être faussée si l'échantillon est contaminé par des protéines ou de l'ARN. Pour cette raison, il est indispensable de mesurer également l'absorbance à 280nm (pic d'absorption des acides aminés aromatiques tels que la Tyrosine et le Tryptophane).
Le calcul du rapport A260/A280 permet d'évaluer la pureté de l'échantillon.
- Si le rapport est compris entre 1,8 et 2 l'ADN est de bonne qualité
- Si le rapport est <1,8 : l’ADN est contaminé par des protéines
- Si le rapport est >2 : l’ADN est contaminé par des ARN.
Une mesure à 230nm permet de détecter d'autres contaminants comme les solvants organiques.
Exemple:
On veut estimer la concentration et la pureté d'un ADN avec les mesures d'absorbance suivantes :
- Abs260nm=0,188 et
- Abs280nm=0,097.
Calculs:
La concentration en ADN est égale à Abs260nm x 50, donc 0,188 x 50 = 9,4 ng/µL
La pureté est estimée avec le rapport Abs260nm/Abs280nm = 0,188/0,097 = 1,94 soit un degré de pureté satisfaisant car compris entre 1,8 et 2.
Avantages et limites
La mesure d'absorbance est rapide et précise pour des concentrations >2µg/mL et permet de détecter d'éventuels contaminants. Dans le même temps, cette méthode est sensible aux contaminants qui absorbent aux voisinage de 260nm et une surestimation est possible.
Quantification de l'ADN par fluorimétrie
Ce dosage repose sur l'utilisation de colorants fluorescents capables qui se lient spécifiquement à l'ADN. Lorsqu'ils sont excités par une lumière à une longueur d'onde spécifique, ces marqueurs émettent une fluorescence proportionnelle à la quantité d'ADN auquel ils sont liés, ce qui confère à cette méthode une grande sensibilité et une forte spécificité.
Pour quantifier l'ADN par cette méthode, on utilise un kit contenant le colorant fluorescent (par exemple PicoGreen, Qubit). L'échantillon d'ADN est incubé avec le réactif fluorescent quelques minutes puis la fluorescence mesurée à l'aide d'un fluorimètre est déterminée par comparaison avec un standard établi à partir de solutions d'ADN de concentration connues. Plusieurs mesures sont possibles en simultané.
Avantages et limites
La quantification de l'ADN par fluorimétrie est extrêmement précise et spécifique (seul l'ADN est détecté). De plus, cette méthode est particulièrement sensible en étant capable de détecter des quantités 'ADN aussi faible que 10ng/mL.
Cependant, la quantification par fluorimétrie nécessite l'utilisation de kits et d'un fluorimètre qui nécessite un investissement important.
Comparatif des méthodes de quantification de l'ADN
| Critères | Gel d'agarose | Spectro. UV | Fluorimétrie |
| Précision | faible | moyenne | très élevée |
| Spécificité | moyenne | faible | élevée |
| Sensibilité | faible (5µg/mL) | moyenne (2µg/mL) | très élevée (10ng/mL) |
| Rapidité | non | très rapide | rapide |
| Evaluation de la pureté | non | oui | non |
| Evaluation de l'intégrité | oui | non | non |
| Coût | faible | modéré | élevé |
| Remarque | permet aussi: vérification visuelle de la taille et de la dégradation |
permet aussi: évaluation de la pureté |
sensibilité et précision élevées mais équipement coûteux |







