Purification d'ADN génomique
Principe
L'ADN génomique peut être extrait et purifié à partir de différents types de cellules: cellules animales, végétales ou bactériennes.
Quelle que soit la source biologique, la purification de l'ADN génomique repose sur trois grandes étapes:
- Lyse cellulaire avec la rupture des membranes et/ou de la parois par détergents ou agents chaotropiques.
- Elimination des autres constituants cellulaires (protéines, lipides, ARN) par digestion enzymatique ou précipitation chimique.
- Purification et concentration de l’ADN, par précipitation à l'alcool ou fixation sur membrane de silice.
Les points critiques sont:
- Eviter la fragmentation mécanique excessive pour préserver l'intégrité des longs ADN,
- Eliminer les contaminants (protéines, lipides, ARN).
Particularités selon le type cellulaire
L'organisation cellulaire varie selon les organismes, ce qui impose l'utilisation de stratégies d'extraction adaptées. Ces différences concernent notamment:
- la présence ou non d'un noyau,
- la nature de la paroi cellulaire,
- la composition des membranes.
Particularités :
- Cellules animales
Chez les cellules animales, l'ADN est contenu dans le noyau, entouré d'une membrane nucléaire et associé à des protéines, principalement des histones. L'extraction de l'ADN nécessite donc la rupture des membranes cellulaires et nucléaire et l'élimination des protéines, des lipides et de l'ARN. - Cellules végétales
L'extraction de l'ADN végétal est plus complexe en raison de la présence d'une paroi cellulaire rigide, riche en cellulose, hémicellulose, lignine et polyphénols. Pour libérer l'ADN, une étape préalable de broyage mécanique, souvent associée à des traitements enzymatiques, est indispensable afin de rompre cette paroi. - Cellules bactériennes
Chez les bactéries, l'ADN n'est pas contenu dans un noyau mais la cellule possède une paroi de peptidoglycane. Cette paroi doit généralement être dégradée à l'aide d'un traitement enzymatique, notamment par le lysozyme, avant la lyse cellulaire.
1 - La lyse cellulaire
Pourquoi la lyse est-elle indispensable ?
La lyse cellulaire permet:
- de rompre les barrières physiques (membranes et parois),
- de libérer l'ADN dans un milieu contrôlé,
- de protéger l’ADN libéré contre l'action des DNases,
- de limiter la contamination par les protéines, les lipides et les polysaccharides.
Méthodes de lyse
Il existe trois grandes familles de méthodes de lyse, qui sont souvent combinées:
| Type de lyse | Méthode (exemple) | Avantages | Inconvénients |
| Mécanique | Broyage, sonication, congélation-décongélation | Méthode universelle, efficace sur les parois rigides | Risque de fragmentation de l'ADN |
| Chimique | Détergents (SDS, Triton X-100), solvants | Rapide, efficace sur les membranes | Toxicité, inhibition possible des enzymes |
| Enzymatique | Lysozyme, protéinase K, cellulase | Spécifique, douce pour l'ADN | Coût, temps d'incubation |
Choix de la méthode selon l'origine de l'échantillon
Chaque type cellulaire présente des structures d'enveloppes différentes (membrane simple, paroi en polysaccharides, parois de peptidoglycanes, etc...) qui nécessitent des stratégies adaptées. Nous présentons ici les exemples les plus fréquemment rencontrés.
Cellules animales
La lyse des cellules animales est relativement simple, avec:
- détergents (SDS, Triton X-100) pour solubiliser les membranes,
- tampon hypotonique pour favoriser l'éclatement cellulaire,
- EDTA pour chélater les cations bivalents (Mg²⁺) et inhiber les DNases,
- protéinase K pour digérer les protéines (histones, nucléases).
Cellules végétales
La lyse des cellules végétales est plus complexe, avec:
- broyage mécanique (souvent à l'azote liquide).
- enzymes spécifiques (cellulase, parfois pectinases).
- tampon CTAB (Bromure de Cétrimonium) pour précipiter les polysaccharides.
- PVP (polyvinylpyrrolidone) pour piéger les polyphénols oxydants.
2 -Purification de l'ADN
Principe
Le choix de la méthode de purification de l'ADN dépend:
- de l'utilisation prévue en aval (PCR, clonage, séquençage),
- du niveau de pureté requis,
- du rendement attendu,
- des contraintes de sécurité et de temps.
| Méthodes | Principe | Avantages | Inconvénients | Utilisation en clonage |
| Extraction au phénol-chloroforme |
Séparation par solvants organiques | Très grande pureté | Solvants toxiques, procédure longue | Possible avec précautions |
| Purification sur silice (colonnes ou billes) |
Adsorption sélective de l'ADN | Rapide, reproductible | Coût | Idéale |
Extraction chimique au phénol-chloroforme
Le mélange phénol-chloroforme dénature les protéines, qui migrent dans la phase organique, tandis que l'ADN reste dans la phase aqueuse.
Après centrifugation, on obtient 3 phases :
- une phase aqueuse supérieure contenant l'ADN,
- une interphase contenant les protéines dénaturées,
- une phase organique inférieure contenant les solvants et les lipides.
Méthode
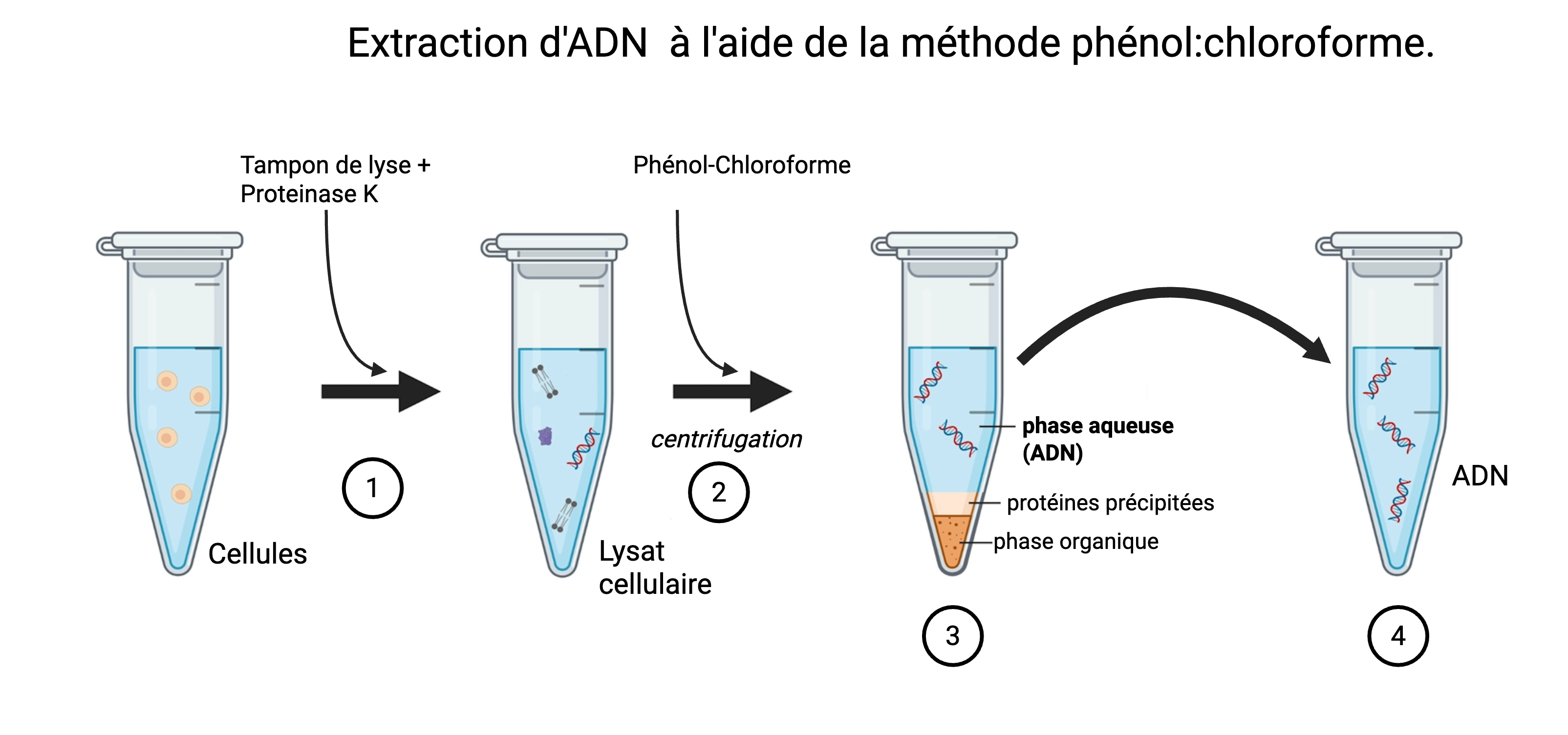
Etapes clefs
- Récupération du lysat cellulaire,
- Ajout de phénol:chloroforme:alcool isoamylique (25:24:1),
- Agitation puis centrifugation à haute vitesse,
- Récupération de la phase aqueuse (ADN).
Un volume égale de chloroforme seul est ajouté pour éliminer tout résidu de phénol et de nouveau traité (étapes 3 et 4).
L’ADN est ensuite précipité à l’éthanol.
Avantages et limites
Cette méthode permet d'obtenir un ADN de très grande pureté. Cependant, le phénol et le chloroforme sont volatils et hautement toxiques et peuvent inhiber certaines applications en aval (ex: PCR).
Extraction en phase solide sur silice
Cette méthode de purification repose sur l'utilisation de sels chaotropiques (guanidium) qui favorisent la liaison de l'ADN à la silice.
Mini colonne de centrifugation
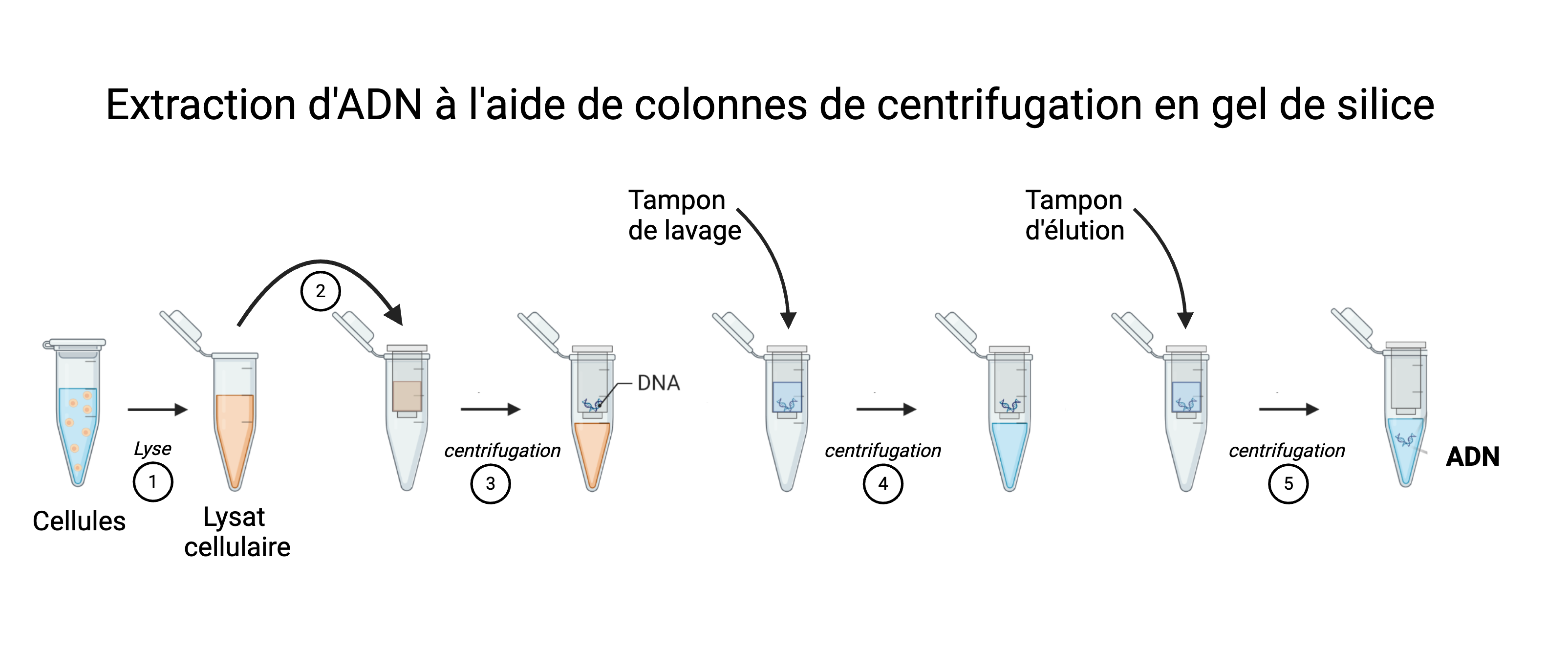
Les étapes clefs
- Chargement du lysat cellulaire,
- Fixation de l'ADN sur la membrane,
- Lavages successifs (sels et éthanol)
- Séchage,
- Elution de l'ADN dans un tampon pauvre en sels ou dans l'eau.
Billes magnétiques
Une autre méthode d’extraction en phase solide utilise des billes magnétiques, recouvertes de silice, qui présentent l'avantage de ne pas nécessiter de centrifugation et être facilement automatisables.
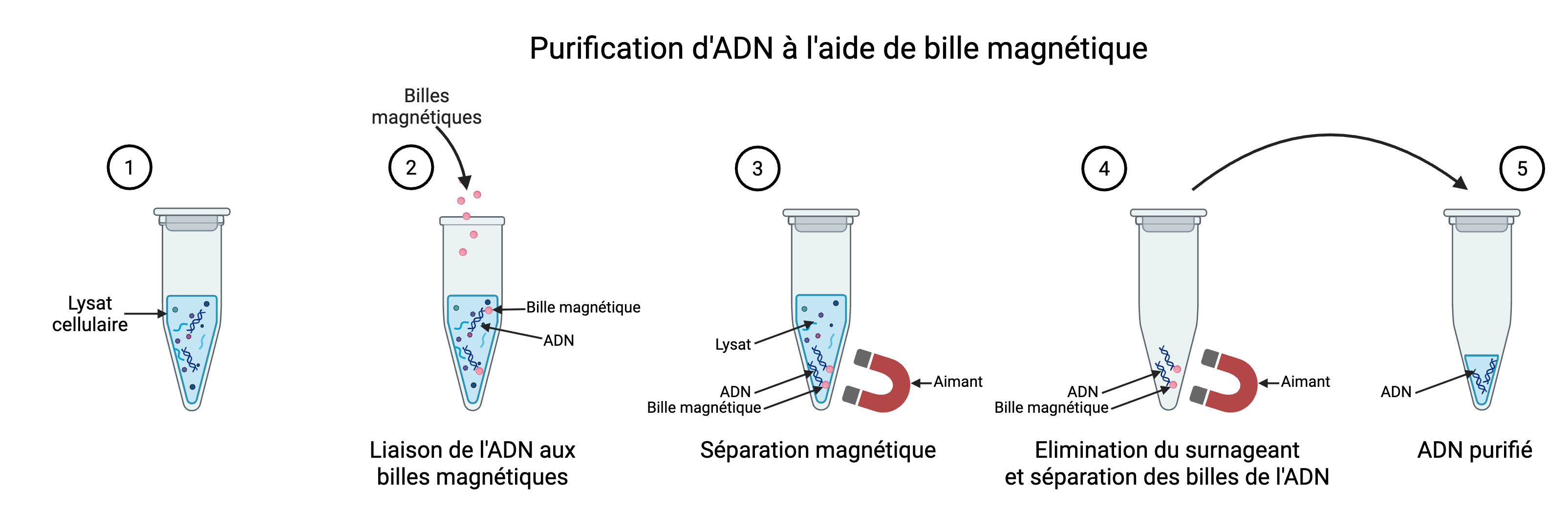
Les étapes clefs
- Chargement du lysat cellulaire,
- Fixation de l'ADN sur les billes,
- Lavages successifs (sels et éthanol), les billes (ADN) sont retenues par un aimant,
- Séparation de l'ADN des billes,
- Elution de l'ADN dans un tampon pauvre en sels ou dans l'eau.
3 - Précipitation et concentration de l'ADN purifié
Principe
La précipitation à l'éthanol permet de concentrer et dessaler les préparations d'ADN.
Elle repose sur:
- La neutralisation des charges négatives de l'ADN par des cations monovalents,
- La diminution de la polarité du solvant par l'alcool.
Méthode
Après l'étape de purification, l'ADN peut être précipité pour être concentré et/ou déssalé.
Les principales étapes sont :
- Ajout d'NaOAc (acétate de sodium) ou de NH4OAc (acétate d'ammonium).
- Ajout de 2 à 2,5 volumes d'éthanol froid à 100%,
- Incubation à -20°C ou -80°C,
- Centrifugation et élimination du surnageant,
- Lavage du culot dans de l’éthanol 70%,
- Séchage et remise en suspension de l'ADN dans un tampon adapté.
L'ajout de RNase est recommandé afin d'éliminer les ARN contaminants. Les ribonucléotides issus de la dégradation de l'ARN restent en solution tandis que l'ADN précipite.







