Les vecteurs de clonage
Le clonage nécessite des éléments capables de transporter et d'amplifier l'ADN d'intérêt. Ces éléments sont appelés vecteurs de clonage. Leur structure et leurs propriétés conditionnent la réussite du clonage.
Ce chapitre décrit les différents types de vecteurs (plasmides, phages, cosmides, chromosomes artificiels).
Définition
Un vecteur de clonage est une molécule d’ADN, le plus souvent modifiée artificiellement, capable de:
- se répliquer de manière autonome dans une cellule hôte,
- transporter et maintenir un fragment d'ADN étranger (insert).
Pour ce faire, le vecteur doit posséder:
- une origine de réplication (ori) compatible avec la cellule hôte,
- un ou plusieurs gènes de sélection qui permettent d'identifier les cellules transformées,
- au moins un site de clonage, souvent intégré dans un site multiple de clonage, pour insérer l'ADN à cloner.
Les différents vecteurs de clonage
Le choix du vecteur dépend en particulier:
- de la taille du fragment d'ADN à cloner,
- de la compatibilité avec la cellule hôte (bactérie, levure, cellule animale, végétale...),
- du mode de sélection souhaité,
- du nombre de copies du vecteur par cellule,
- de l'objectif : clonage, expression du gène, construction de banque...
1- Les plasmides
Les plasmides naturels sont de petites molécules d'ADN circulaire double brin, capables de se répliquer indépendamment de l'ADN chromosomique de la cellule hôte qu’ils parasitent. Ils peuvent être facilement purifiés en grande quantité.
Ils peuvent insérer des ADN étrangers de taille réduite, généralement inférieure à 10 kpb.
Propriétés des plasmides de laboratoire
Les plasmides utilisés en laboratoire sont des plasmides naturels génétiquement modifiés. Ils sont utilisés pour:
- le clonage de fragment d'ADN de petite taille (<10kpb),
- le sous-clonage,
- la construction de banques d'ADNc,
- l'expression de gènes (avec des plasmides d'expression).
Le plasmide pBR322
Le pBR322 est un plasmide référence utilisé chez E.coli.
Il se multiplie dans la bactérie en 10 à 20 copies en condition normale de croissance.
Il porte deux gènes qui confèrent la résistance aux antibiotiques: le gène bla (pour résistance à l'Ampicilline) et le gène tet (pour la résistance à la Tetracycline).
Il possède plusieurs sites de restriction uniques (EcoRI, EcoRV, BamHI, PstI, PvuI et HindIII).
A noter que les sites BamHI et PstI sont localisés respectivement dans les gènes tet et bla. Ainsi, l'insertion d'un ADN étranger dans l'un des ces sites provoque l'inactivation du gène de résistance correspondant, permettant une sélection par inactivation insertionnelle.
Les plasmides pUC18 et pUC19
pUC18 et pUC19 sont des plasmides circulaires double brin, dérivés de pBR322 et du bactériophage M13.
Ces vecteurs portent
- le gène de résistance à l'ampicilline (bla),
- une origine de réplication à haut nombre de copies,
- le fragment lacZ alpha qui code pour la région N-terminale de la beta-galactosidase,
- Le site multiple de clonage (SMC) est inséré dans le gène lacZ alpha. Ainsi, l'insertion d'un ADN étranger entraîne la perte d'activité de la beta-galactosidase, détecté par le test blanc/bleu sur milieu X-gal/IPTG.
La différence entre pUC18 et pUC19 réside uniquement dans l'orientation inverse du SMC.
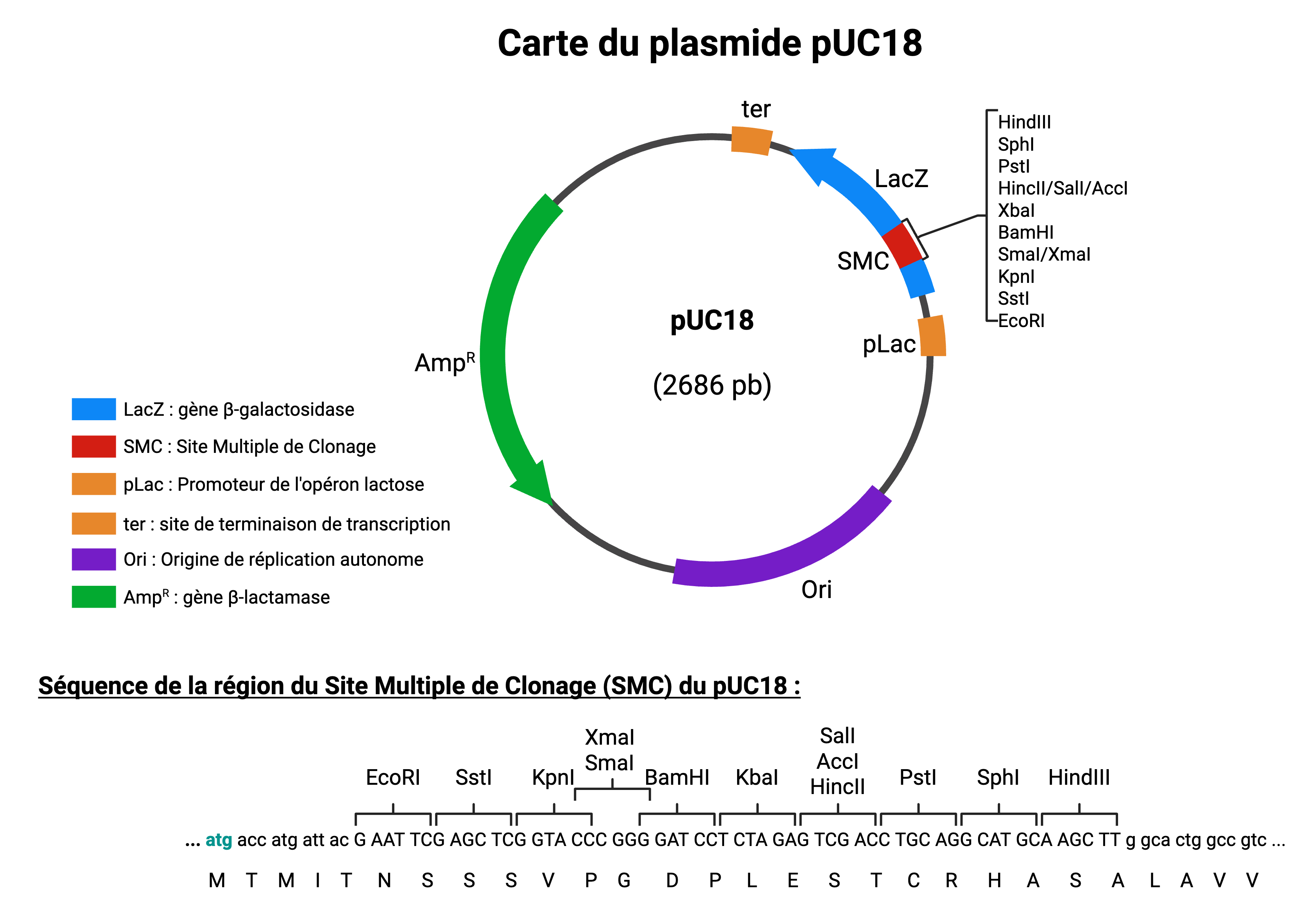
Plasmide pUC18
Le tableau suivant présente les éléments constitutifs d’un plasmide de laboratoire (exemple du plasmide pUC18):
| Elément plasmidique | Fonction |
|---|---|
| Origine de réplication (ori) | Permet la réplication autonome du plasmide dans la bactérie hôte. |
| Site de clonage multiple (SMC/CMS) | Regroupe pluseiurs sites de restriction uniques permettant l'insertion de l'ADN d'intérêt. |
| Gène de résistance aux antibiotiques | Sert de marqueur de sélection des bactéries transformées. |
| Gène rapporteur (marqueur) | Permet le criblage des clones recombinants (ex: LasZ). |
| Promoteur | Initie la transcription du gène cloné (dans les plasmides d'expression). |
| Site RBS | Permet la traduction du gène cloné (dans les plasmides d'expression). |
| Site terminateur (Ter) | Stoppe la transcription du gène cloné (dans les plasmides d'expression). |
| Site de liaison d'amorces 5' et 3' | Utilisés pour la PCR et le séquençage de l'ADN cloné. |
2- Les vecteurs dérivés du phage
Les bactériophages
Les bactériophages sont des virus qui infectent les bactéries. Ils sont utilisés comme vecteur de clonage pour
cloner des ADN plus grands que ceux clonés par des plasmides.
Ils bénéficient d'une efficacité de transfert très élevée par infection.
Pour ces raisons, les bactériophages sont particulièrement adaptés pour la construction de banques d'ADNc et d'ADN génomiques.
-
Le phage λ (lambda)
Le phage λ (lambda) est couramment utilisé en laboratoire.
L'ADN double brin linéaire du phage λ présente des extrémités cohésives (cos) qui permet sa circularisation dans la bactérie hôte.
Il peut se multiplier selon deux modes différents: cycle lytique et cycle lysogénique. Pour les expériences de clonage, seul le cycle lytique est utilisé car il permet de produire un grand nombre de phages.
Lors du clonage, les régions centrales non essentielles du génome sont remplacées par un insert étranger (10 à 20 kpb).
De plus, des phages λ modifiés (ex: phage λ11) permettent la sélection et le criblage des clones recombinants.
-
Le phage M13
Le bactériophage M13 possède un génome d'ADN simple brin circulaire et n'entraine pas de lyse bactérienne. Il est utilisé pour:
- le clonage de petits fragments d’ADN,
- le séquençage Sanger (historiquement),
- la production d'ADN simple brin,
- certaines techniques de mutagenèse dirigée.
Les phagemides
Les phagemides sont des vecteurs hybrides qui combinent les caractéristiques d'un plasmide et d'un bactériophage. Ils présentent :
- une origine de réplication plasmidique,
- une origine de réplication phagique (souvent dérivée du M13)
- un gène de résistance,
- un site multiple de clonage
Ils peuvent être :
- répliqués comme des plasmides
- être encapsidés dans des particules phagiques en présence d'un phage auxiliaire.
Comme pour les plasmides, les phagemides permettent le clonage d'ADN d'environ 10kpb.
Les cosmides
Les cosmides sont des vecteurs hybrides combinant des éléments de plasmides et la séquence cos du phage λ:
- origine de réplication, gène de sélection et site multiple de clonage d'origine plasmidique,
- les séquences cos du phage λ qui permettent l'encapsidation de l'ADN facilitant l'infection bactérienne.
Ainsi, les cosmides permettent le clonage de fragments de 28 à 45 Kb et sont utilisés pour les banques génomiques, en revanche, ils ne sont pas adaptés à l'expression des gènes.
3- Les chromosomes artificiels
Chromosome artificiel bactérien (BAC)
Les BAC sont dérivés du plasmide F d'E.coli impliqué dans la conjugaison bactérienne. Ils fonctionnent comme des plasmides de très grande taille.
Ils ont une très grande capacité de clonage jusqu'à 300 à 500 kpb,
Ils sont très stables, mais en faible nombre de copies (1 à 2 copies par cellule).
Leur grande stabilité en font des vecteurs de choix pour les projets de séquençage des génomes et la cartographie physique.
Chromosome artificiel de levure (YAC)
Les YAC sont conçus pour être utilisés dans les levures comme Saccharomyces cerevisiae.
Les YAC fonctionnent comme de véritables chromosomes eucaryotes, avec :
- une ARS (origine de réplication),
- un centromère,
- deux télomères,
- des gènes de sélection pour la levure.
Ils permettent le clonage de fragments d’ADN eucaryote très longs, de 200kpb à 1 mégabase (1Mb=1000kb) mais présentent une instabilité génétique, ce qui conduit à leur remplacement progressif par les BAC.
4- Vecteurs d'expression eucaryotes
Les vecteurs viraux animaux.
Les vecteurs viraux animaux permettent le transfert et l'expression de gènes eucaryotes avec modifications post-traductionnelles. Ce qui n'est pas possible avec les systèmes procaryotes qui ne permettent pas les modifications post traductionnelles comme la glycosylation, la phosphorylation ou le repliement correct des protéines.
Les gènes viraux pathogènes sont supprimés et remplacés par l'ADN d'intérêt.
Les vecteurs viraux les plus utilisés, sont:
- les adénovirus, pour une expression transitoire,
- les retrovirus, les lentivirus pour une intégration stable,
- les virus adéno-associés (AAV).
Les vecteurs viraux animaux permettent un haut rendement de transduction mais nécessitent des conditions strictes de biosécurité. Ils sont utilisés en recherche fondamentale, en biotechnologie et en thérapie génique.
Les vecteurs viraux végétaux
Les vecteurs viraux végétaux sont dérivés de virus infectant naturellement les plantes, par exemple:
- le virus de la mosaïque du tabac (TMV) qui permet une expression transitoire élevée,
- le plasmide Ti d'Agrobacterium tumefaciens qui permet une intégration stable du transgène dans le génome de la plante.
Les vecteurs viraux végétaux sont utilisés pour la production de protéines recombinantes, l'étude fonctionnelle des gènes et l'amélioration génétique des plantes.
Tableau récapitulatif
| Vecteur | Taille de l'insert | Cellule hôte | Avantages | Inconvénients |
|---|---|---|---|---|
| Plasmide | <10kpb | Bactérie | Manipulation simple, faible coût. | Taille limité de l'insert. |
| Phagémide | environ 10kpb | Bactérie | Double mode plsmide/phage. Production d'ADN simple brin. Bonne efficacité. | Nécessite un phage auxilliaire. Taille limitée de l'insert. |
| Phage Lambda | <20kpb | Bactérie | Très bonne effocacité d'infection. Idéal pour banque génomique/ADNc. | Manipulation complexe. Pas adapté à l'expression. |
| Phage M13 | <5kpb | Bactérie | Production d'ADN simple brin, mutagénèse dirigée, séquençage. | Petite taille de l'insert. |
| Cosmide | 28-45 kpb | Bactérie | Grands fragments. Infection efficace, stabilité. | Expression génique difficile. |
| BAC | 300-500 kpb | Bactérie | Très stable. Grands fragments. Idéal pour analyse des génomes. | Faible nombre de copies. Manipulation délicate. |
| YAC | <1 Mpb | Levure | Très grands fragments. Comportement eucaryote. | Instabilité génétique. Réarrangements fréquents. |
| Vecteurs viraux animaux | 5 à 30 kpb | Cellules animales | Expression efficace. Modifications post-traductionelles. Transduction élevée. | Coût élevé, biosécurité stricte. Taille limitée de l'insert. |
| Vecteurs viraux végétaux | 5 à 25 kpb | Cellules végétales | Expression rapide. Applications agronomiques. | Taille limitée de l'insert. |







