Transformation bactérienne
La transformation permet l'introduction du plasmide recombinant dans une bactérie hôte compétente, afin de permettre la propagation, la sélection et éventuellement l'expression du gène cloné.
Ce chapitre décrit les méthodes de transformation :
- soit par un traitement chimique suivi d'un choc thermique,
- soit par électroporation.

Transformation chimique suivie d'un choc thermique
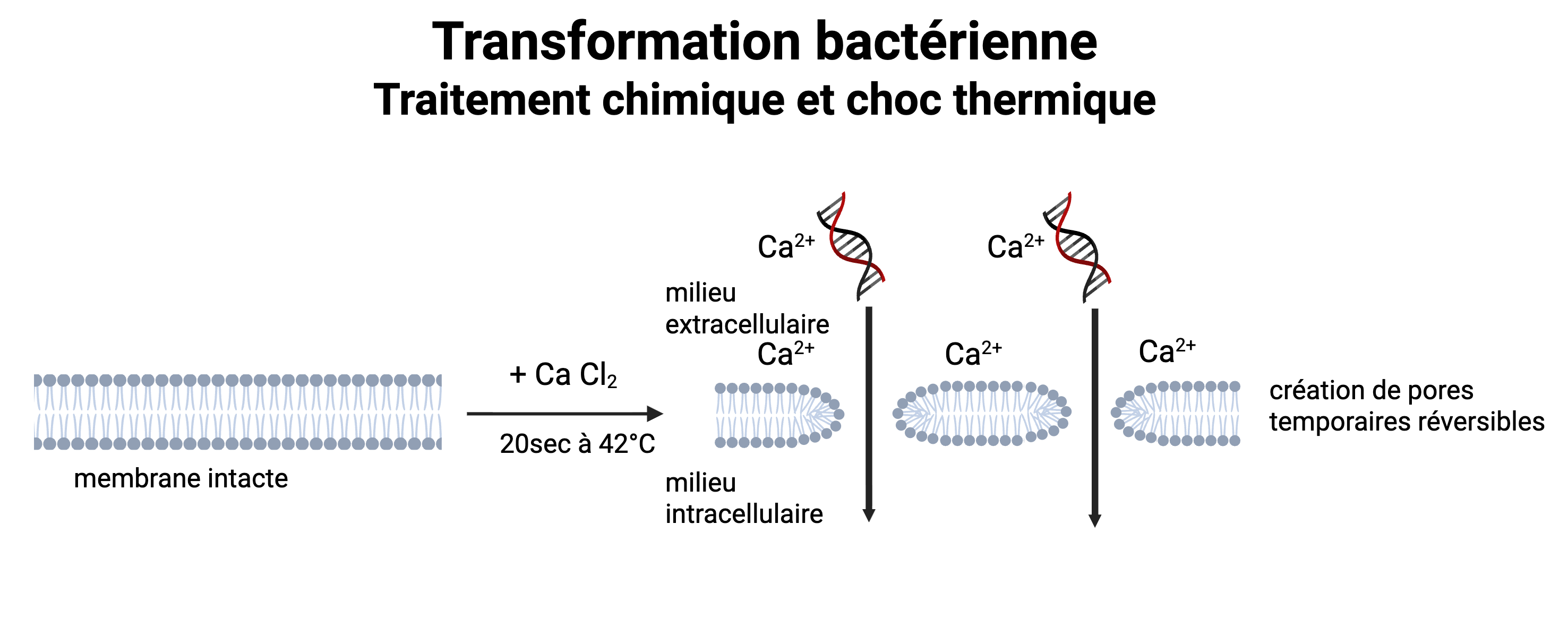
La transformation chimique repose sur un traitement des bactéries par des ions calcium (Ca2+). Ces ions neutralisent partiellement les charges négatives portées à la fois :
- par la membrane bactérienne, et
- par l'ADN (groupements phosphates),
ce qui réduit la répulsion électrostatique entre les l'ADN et la membrane cellulaire.
Le choc thermique provoque ensuite une augmentation brutale de la fluidité membranaire, favorisant la formation de pores transitoires à travers lesquels l'ADN plasmidique peut pénétrer dans la cellule.
Protocole de transformation par choc thermique
- Décongélation des cellules compétentes
Les bactéries compétentes préparées par induction chimique puis stockées à -80°C, sont décongelées lentement. - Incubation avec l'ADN
Le produit de ligation est ajouté aux cellules compétentes puis le mélange est incubé sur glace pendant 15 à 30 minutes.
Cette étape favorise l'association de l'ADN plasmidique avec la surface des bactéries. - Choc thermique
Les cellules sont soumises à un choc thermique bref (30 à 60 sec à 42°C), puis immédiatement replacées sur glace.
Cette variation rapide de température facilite l'entrée de l'ADN dans les cellules et son piégeage à l'intérieur. - Phase de récupération
Les bactéries sont incubées à 37°C dans un milieu nutritif non sélectif pendant 30 minutes à une heure.
Cette étape permet: la réparation de la membrane bactérienne et l'expression des gènes porté par le plasmide, notamment le gène de résistance à l'antibiotique. - Sélection des cellules transformées
Les bactéries sont étalées sur des boîtes de Pétri contenant un milieu sélectif supplémenté avec l'antibiotique approprié. Seules les bactéries transformées forment des colonies. (voir § Sélection et Criblage).
Transformation par électroporation
L'électroporation consiste à soumettre les bactéries à une impulsion électrique brève et intense. Le champ électrique crée des pores transitoires dans la membrane bactérienne, permettant l'entrée de l'ADN plasmidique.
Cette méthode est plus efficace que le choc thermique mais elle nécessite un équipement spécifique.

Protocole de transformation par électroporation
- Décongélation des cellules compétentes
Les bactéries compétentes (dépourvues de sels) préparées au préalable et stockées à -80°C, sont décongelées lentement. - Mélange avec l'ADN
L'ADN plasmidique est ajouté aux cellules électrocompétentes dans un faible volume, afin de limiter la conductivité du milieu. - Impulsion électrique
Le mélange est placé dans une cuvette d'électroporation, puis soumis à une impulsion électrique contrôlée, entraînant des pores transitoires dans la membrane. - Phase de récupération
Immédiatement après l'impulsion, les bactéries sont incubées à 37°C dans un milieu nutritif non sélectif pendant 30 minutes à une heure. - Sélection des cellules transformées
Les bactéries sont étalées sur des boîtes de Pétri contenant un milieu sélectif supplémenté avec l'antibiotique approprié. Seules les bactéries transformées forment des colonies. (voir § Sélection et Criblage).
Comparaison des méthodes
Le choix de la méthode de transformation dépend des objectifs expérimentaux, du type de bactérie utilisée et des ressources disponibles.
| Méthodes de transformation | Avantages | Limites |
| Choc thermique | Simple, peu coûteuse, adaptée aux plasmides de petite taille | Efficacité limitée |
| Electroporation | Très haute efficacité, applicable à de nombreuses souches bactériennes | nécessite un équipement spécifique, cellules plus fragiles |







