Enzymes de restriction et sites de restriction
Définition
Les enzymes de restriction (ER) sont des endonucléases d’origine bactérienne capables de reconnaître et d'hydrolyser l'ADN au niveau de séquences spécifiques appelées sites de restriction.
Ce sont des outils essentiels pour la manipulation précise et reproductible de l'ADN pour le clonage moléculaire.
1- Les enzymes de restriction
Système restriction/modification
Chez les bactéries, les enzymes de restriction font partie du système de défense (restriction/modification) contre les bactériophages.
Ainsi, les enzymes de restriction hydrolysent sélectivement l'ADN étranger non méthylé sans attaquer l'ADN bactérien qui est protégé par la méthylation de bases au niveau des sites de restriction.
Pour ce système de restriction/modification, on a donc:
- une enzyme de restriction, qui hydrolyse l'ADN étranger non méthylé,
- une méthylase associée qui protège l'ADN bactérien en méthylant les mêmes séquences sur l'ADN bactérien afin de le protéger de l'hydrolyse.
Classification des enzymes de restriction
Il existe plusieurs classes (types) d'enzymes qui diffèrent par leur structure, leurs besoins en cofacteur, leurs modes d’action et la localisation du site d'hydrolyse.
Type I (peu utilisées):
- Reconnaissance d'une séquence spécifique
- Hydrolysent l'ADN à distance variable du site reconnu
- Nécessitent de l'ATP et du Mg2+
- Sont des complexes enzymatiques
Type II (outils principal en biologie moléculaire):
- Hydrolysent l'ADN au niveau ou à proximité immédiate du site reconnu
- Nécessitent uniquement du Mg2+
- Ont généralement une structure dimérique
- Produisent une hydrolyse prévisible et reproductible
Type III :
- Reconnaissance d'une séquence spécifique
- Hydrolysent à 25-30 pb en aval du site reconnu
- Nécessitent de l'ATP et du Mg2+
Type IV :
- Hydrolysent de préférence des ADN méthylés ou modifiés
- Type V (CRISPR-Cas) :
- Guidés par un ARN pour hydrolyser une séquence.
- Outils modernes d'édition du génome
En biologie moléculaire, les enzymes de type II sont quasiment exclusivement utilisées.
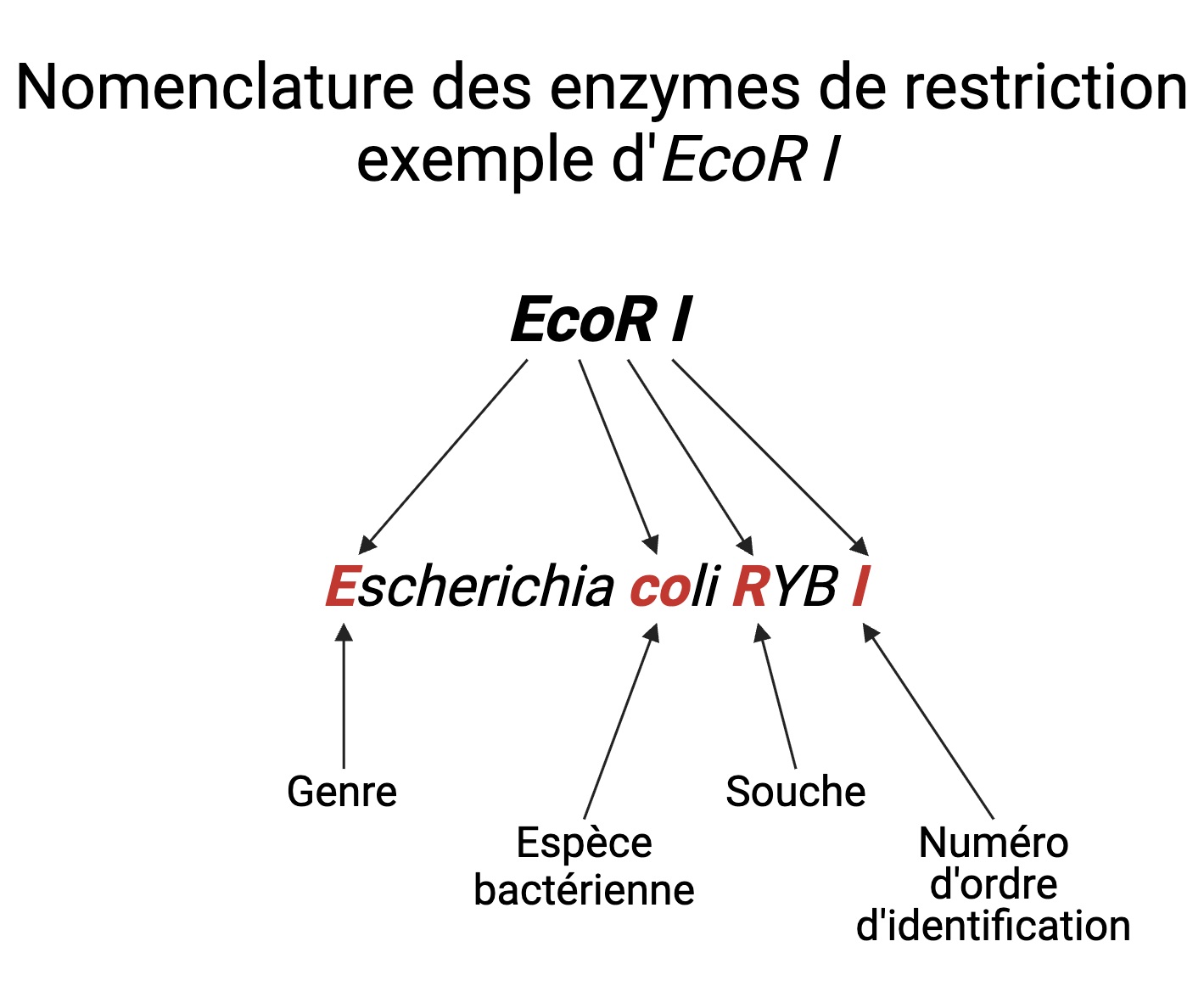
Nomenclature des enzymes de restriction
Le nom d'une enzyme de restriction reflète l'organisme dont elle est issue:
- 1ere lettre (en majuscule) : genre
- 2e et 3e lettres (en minuscules) : espèce
- 4e lettre (optionnelle, en majuscule) :souche
- chiffre romain : ordre de découverte dans cette souche.
Exemple : EcoRI est la 1ere enzyme de restriction isolée à partir de la souche bactérienne Escherichia coli RYB.
2- Les sites de restriction
Les enzymes de restriction de type II reconnaissent des séquences spécifiques de 4, 6 parfois 8 paires de bases, appelées sites de restriction.
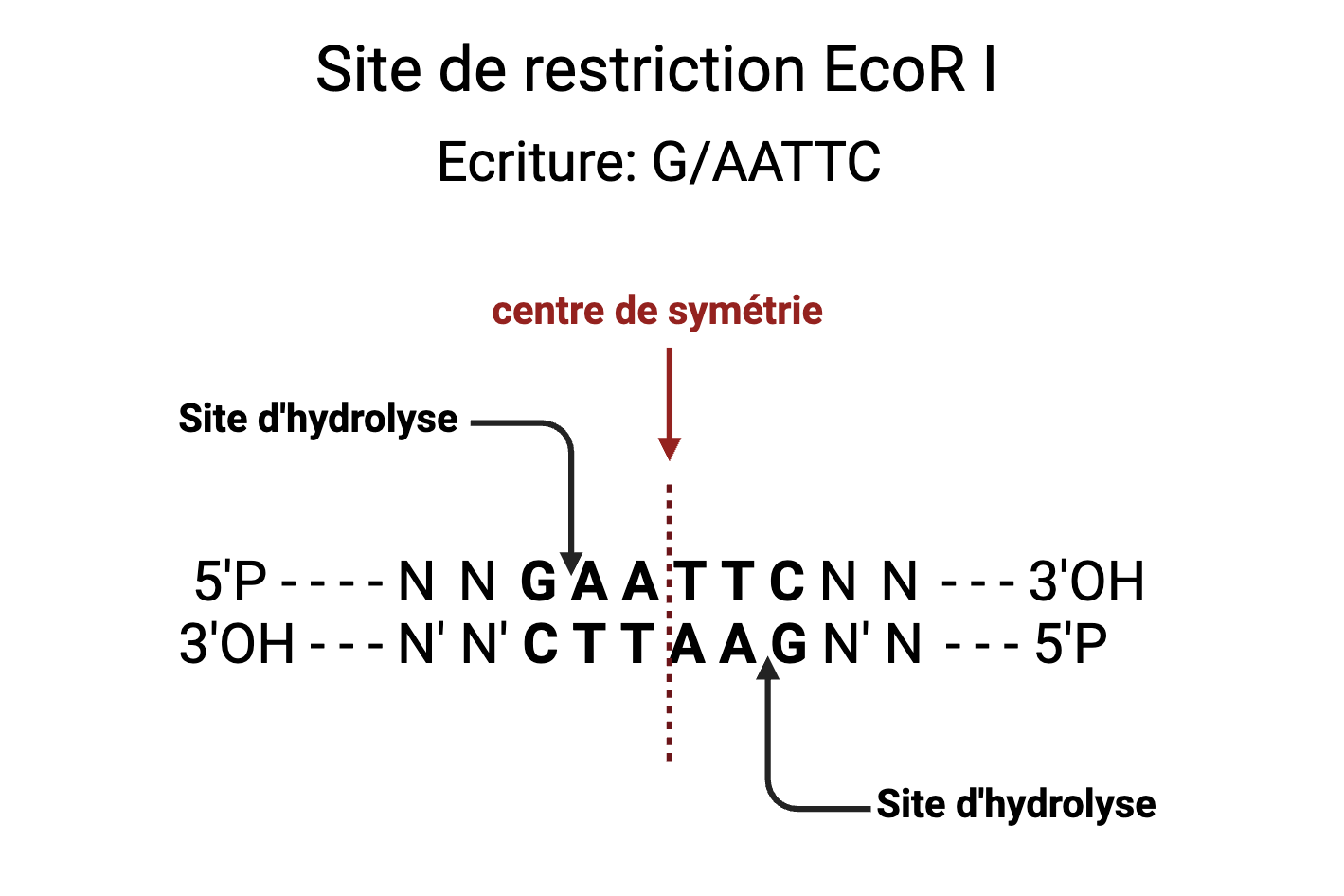
Ces séquences sont généralement palindromiques, c'est à dire qu'en lisant chaque brin (de 5’ vers 3’) on obtient la même séquence (palindrome à répétition inversée). Le site présente donc un axe de symétrie (voir figure suivante, le site EcoRI : G/AATTC).
Les sites peuvent inclure des bases ambiguës (code IUPAC):
- R = A ou G
- Y = C ou T
- N = n'importe quelle base, permettent à une enzyme de reconnaître plusieurs variantes de séquence.
Convention d’écriture d’un site de restriction
Compte-tenu de la complémentarité des bases sur les deux brins d’ADN, une écriture simplifiée de la séquence du site de restriction est utilisée (voir exemple du site EcoRI (G/AATTC)):
- On note uniquement la séquence du brin supérieur lue de 5' vers 3'.
- L’orientation du brin (5’ à gauche vers 3’ à droite) n’est pas précisée car elle est implicite
- Le site d’hydrolyse est indiqué par une barre oblique ou une flèche placée entre les 2 nucléotides cibles.
Isoschizomères
Les isoschizomères sont des enzymes de restriction différentes qui reconnaissent la même séquence ADN.
On distingue les isoschizomères:
-
Vrais:
- même site
- même hydrolyse
Par exemple, SstI (GAGCT/C) et SacI (GAGCT/C).
-
Partiels :
- même site
- hydrolysent à un site différent
Par exemple, Asp718 (G/GTACC) et KpnI (GGTAC/C).
-
Sensibles à la méthylation
- même site
- l'activité dépend de l'état de méthylation du site.
Par exemple, MspI (C/CGG) qui hydrolyse le site sous forme méthylée* (C/CmGG) ou non, et l’enzyme HpaI (C/CGG) qui n’hydrolyse que la forme non méthylée.
*(Cm: Cytosine méthylée)
Fréquence de coupure
Plus un site est long, plus la fréquence d'avoir cette séquence est faible, donc plus rare est l'hydrolyse possible de ce site.
- Site à 4pb: hydrolyse en moyenne toutes 256pb (=44)
- Site à 6pb: hydrolyse en moyenne toutes 4096pb (=46)
- Site à 8pb: hydrolyse en moyenne toutes 65536pb (=48)
Cette notion est importante pour choisir une enzyme de restriction selon le niveau de fragmentation souhaité.
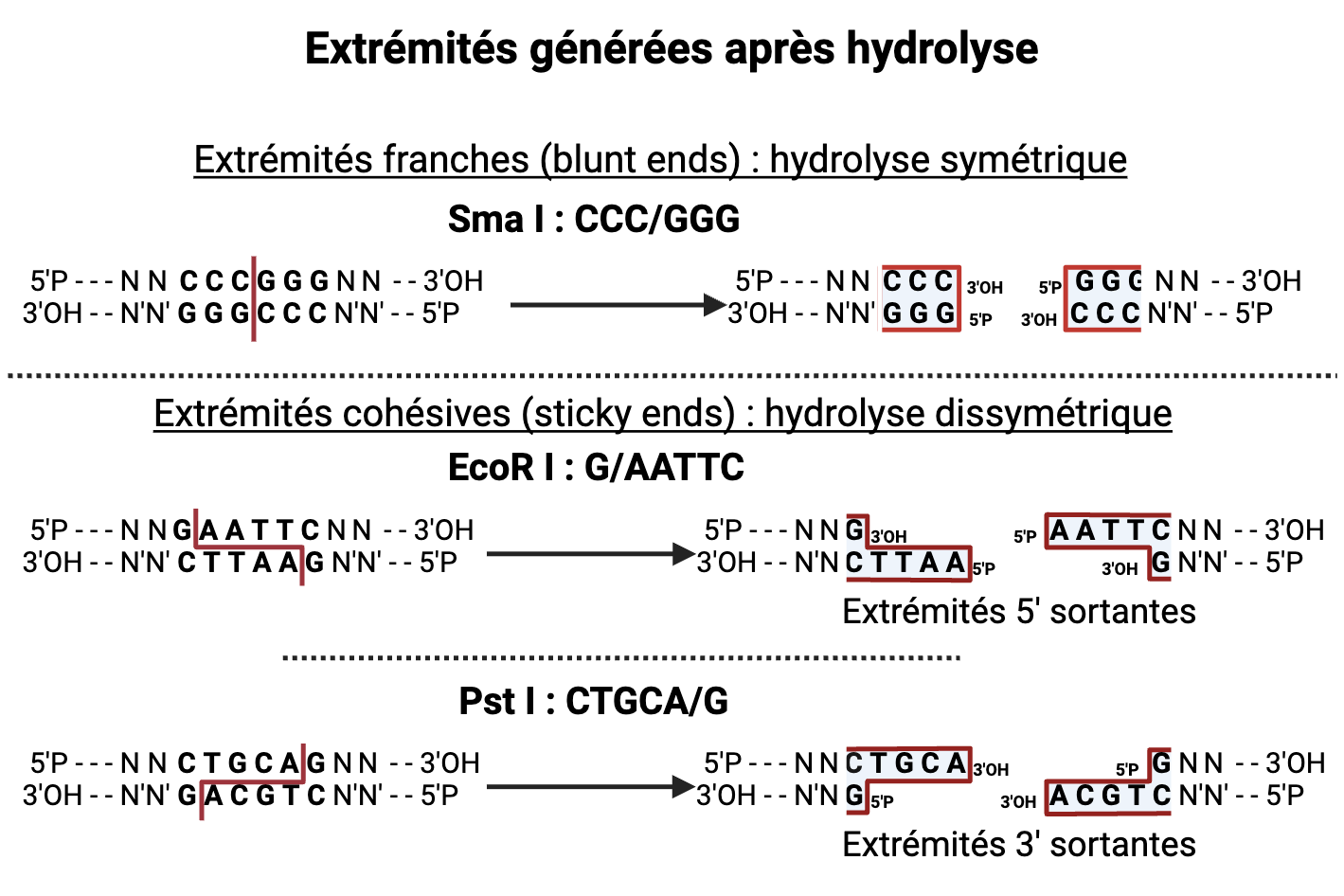
Types d'extrémités générées
Selon la position du site d’hydrolyse par rapport à l'axe de symétrie du site de restriction, on distingue :
Extrémités cohésives ou bouts collants (sticky ends)
- 5' sortantes (ex : EcoRI)
- 3' sortantes (ex : PstI)
Si les sites d’hydrolyse sont décalés par rapport à l'axe de symétrie.
Extrémités franches (blunt ends)
- aucune portion simple brin (ex : SmaI)
Si les sites d’hydrolyse sont au niveau de l'axe de symétrie.
Ces extrémités conditionnent l'efficacité de la ligation. Les extrémités cohésives pouvant s'hybrider, les nucléotides entre lesquels la ligase doit créer la liaison phosphoester sont rapprochés ce qui facilite la ligation de ce type d'extrémités par rapport aux extrémités franches.